دکتر Poul Martin در حال نشان دادن ساختارهای انگشت مانند به نام filopodia است، که بیرون زدگیهای لولهای شکل در غشای سلولی هستند. آنها میتوانند محیط شیمیایی و فیزیکی را با استفاده از حسگرهای بسیار حساس شناسایی کنند.
سلولها دارای برآمدگیهای انگشت مانندی هستند که برای حس کردن اطراف خود به کار میبرند. آنها با استفاده از حسگرهای بسیار حساس میتوانند محیط شیمیایی و فیزیکی اطراف خود را حس کنند. تحقیق جدیدی که بهوسیله پژوهشکده Niels Bohr انجام شده است نشان میدهد که چگونه این ساختارهای انگشت مانند به نام filopodia میتوانند اندازه خود را زیاد کرده و حرکات پویایی داشته باشند. نتایج این تحقیق در مجله Proceeding of the National Academy of Sciences به چاپ رسیده است.
در ادامه مطلب همراه بیونت باشید
در بسیاری از فرآیندهای زیستی میان کنشهای سلول و ارتباطات با محیط خود برای عملکرد درست بسیار حیاتی میباشد. برای حس کردن اطراف خود، سلولها از ساختارهای انگشت مانندی استفاده میکنند که درواقع بیرون زدگیهای لوله شکلی هستند که از غشا سلولی منشأ میگیرند. این لولهها filopodia نامیده میشوند و میتوانند پیغامهایی را هم درزمینهٔ محیط شیمیایی و هم پوشش فیزیکی اطراف سلول به دست آورند. بهعنوان مثال سلولها از ساختارهای filopodia برای تصحیح تکامل جنین، برای رشد سلولهای عصبی و هنگامی که سلولهایی مانند ماکروفاژها برای مقابله با عوامل بیماریزا نیاز به حرکت بهسوی آنها را دارند استفاده میکنند. پروفسور Poul Martin Bendix در این زمینه میگوید:
«ساختارهای filopodia بسیار پویا بوده و میتوانند جمع شده، طویل شده و به تمام جهات حرکت کنند؛ اما چه چیز به آنها اجازه حرکت میدهد؟ چگونه اطراف خود را کنترل کرده و چه نیروهایی را به کار میبرند؟ این چیزی است که ما میخواستیم کشف کنیم.»
محققان این گروه خصوصیات فیزیکی filopodia را با استفاده از یک تله بصری مورد بررسی قراردادند. این ابزار یک میکروسکوپ است که به کمک آن میتوان بر روی یک سلول زنده توقف کرده و در آن با استفاده از یک لیزر با تمرکز بالا نفوذ کرد، در حالی که میتوانید محیط آنها را مشاهده کرده، سنجیده و دنبال کنید.
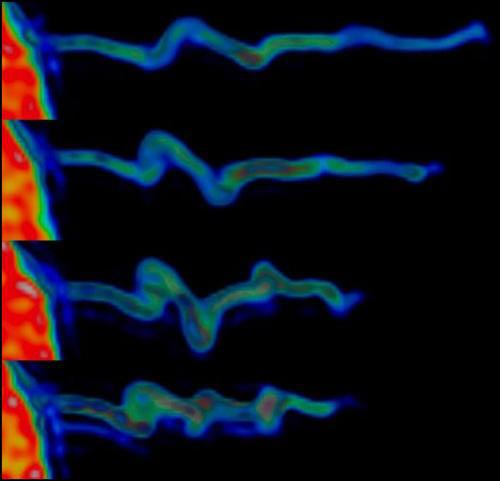
این تصویر نشان میدهد که actin درون filopodia منقبض میشود در حالی که یک ساختار مشخص را تشکیل میدهد. Actin درون filopodium یک جریان چرخشی مشخص را هنگامی که منقبض میشود نشان میدهد و به صورت یک ساختار مارپیچ شکل میشود.
برای پیگیری کردن بهتر حرکات، این محققان یک توپ پلاستیکی کوچک را در نوک ساختار Filopodia قراردادند و با استفاده از سنجشهای نیرویی بسیار حساس توانستند فعالیت پویای هر filopodia را بسنجند. علاوه بر سنجش نیرو، اسکلت درونی filopodia به نام actin که مسئول حرکت filopodia است بهوسیله یک نشانگر فلورسنت نشانگذاری شده و حرکت آن در زیر میکروسکوپ مورد بررسی قرار گرفت.
کشف یک مکانیسم جدید
پرفسور Bendix توضیح داد:
«در این آزمایش ما ابزار توپ مانند را در انتهای filopodia قرار داده و به مدت ۲۰ دقیقه مورد بررسی با میکروسکوپ بسیار حساس به نیرو قراردادیم. توانستیم بفهمیم که سلولها با نیرویی معادل ۱-۱۰۰ پیکونیوتون نیرو وارد میکنند که معادل جاذبه سطحی یک سلول قرمز خون است. علاوه بر این، این مطالعه مکانیسم جدیدی را آشکار ساخت که filopodia برای حرکت به کار میبرد. مشاهده کردیم که actin درون filopodia یک حرکت چرخشی مشخص را نشان میدهد و هنگامی که به عقب کشیده میشود ساختار مارپیچی شکل میگیرد. این فرآیند درست مانند زمانی است که شما یک نوار کشی را پیچانده و یک سر آن را نگه میدارید و سر دیگر را رها کنید.»
این ساختارهای مارپیچ با استفاده از میکروسکوپ فلورسنت هنگام سنجش انقباضها تصویربرداری شدند. مکانیسم چرخشی مارپیچها در ساختارهای actin برای امکانپذیر کردن جابهجایی filopodia در اطراف بسیار مهم است.

شبیهسازی کامپیوتری پویای filopodia نشان داد که یک ساختار چرخشی actin درون لوله به دلیل استحکاک بین غشا و actin اتفاق میافتد و منجر به ایجاد ساختار مارپیچ مشاهده شده میشود.
پروفسور Bendix میافزاید:
«این نتایج جدید یک مکانیسم جدید را نشان میدهد که چرخش به یک تغییر مکانیکی تبدیل شده و به سلولها امکان میان کنش با سلولهای همسایه را میدهد.»
ساختارهای مارپیچی در تمام طبیعت یافت میشوند، مثلاً در رشتههای DNA مارپیچ و تاژکها و مژکهای مو مانند که یک مارپیچ چرخنده میباشند که به بعضی از باکتریها و سلولهای اسپرم امکان حرکت را میدهند.
Filopodia حلقوی پیش از این از لحاظ تئوری پیش بینی شده بود اما این پیشبینیها بر پایه مکانیسمهای متفاوت تشکیل مارپیچ بود. این در حالی است که این ساختارهای مارپیچی جدید میتوانند ازلحاظ تئوری نیز بهوسیله مدلسازی یک ساختار actin درون یک لوله غشادار تأیید شوند. پروفسور Bendix اظهار داشت:
«نتایج ما نشان میدهد که آزمایشها و محاسبات تئوری هنگامی که مکانیسمهای زیستی را مورد مطالعه قرار میدهیم بهخوبی باهم همخوانی دارند.»
منبع: PNAS

