تکنولوژی SLIC یا sequence and ligase independent cloning برای اولین بار توسط Li در سال ۲۰۰۷ ابداع شد و در مجله Nature methods به چاپ رسیده است. اما چه چیز باعث شد که این روش به اندازه Nature methods با ارزش شود؟ بر خلاف دیگر روشهای کلون کردن، SLIC به آنزیمهای محدود کننده و لیگاز نیازی ندارد!!
اگر هنوز باور ندارید میتوانید در ادامه مطلب با بیونت همراه باشید تا با این روش بیشتر آشنا شوید.
چگونه کار میکند
برای کلون کردن با استفاده از SLIC ابتدا باید قطعه DNA مورد نظر را با وسیله PCR تکثیر کنید. شما باید PCR را به وسیله الیگونوکلئوتیدهای طراحی شده اختصاصی انجام دهید. این الیگو نوکلئوتیدها یک توالی ۲۵ جفت بازی در انتهای خود دارند که با انتهاهای وکتور مورد نظر برای کلون کردن (وکتور طراحی شده یا designation vector) همولوگ است. انتهای وکتور در هر سمت که میخواهید محصول PCR را وارد آن کنید از نوع DNA میباشد.
در ادامه انتهاهای مورد نظر را با خطی کردن وکتور ایجاد کنید. میتوانید این کار را با آنزیمهای محدود کننده انجام دهید اما برای افرادی که میخواهند اصلا از آنزیم محدود کننده استفاده نکنند این کار به کمک روش PCR نیز قابل اجرا است.
در مرحله سوم محصولات PCR و وکتور خطی شده را در معرض آنزیم DNA پلیمراز فاژ T4 (در نبود dNTP) قرار دهید. آنزیم پلیمراز با فعالیت ۳’ اگزونوکلئازی خود مشغول ذره ذره هضم کردن وکتور و محصولات PCR شده و شروع به تولید توالی بیرون زده (overhang) در انتهای ۳’ آنها میکند.
با توجه به هضم الیگونوکلئوتیدها، وکتور خطی و محصولات PCR حاوی مناطق همولوگ میشوند. این توالی بیرون زده، وکتورها و محصولات PCR را مانند قطعاتی میکند که انگار از ابتدای آفرینش برای هم ساخته شده باشند، یا شاید هم در آزمایشگاه شما!!!!.
پس از اینکه وکتور خطی و محصول PCR طول مناسبی از توالی تک رشته ای ۵’ مکمل را به دست آوردند، dCTP را به واکنش اضافه میکنیم. اضافه کردن dCTP باعث فعال شدن خاصیت پلیمرازی DNA پلیمراز T4 میشود. اما از آنجایی که تنها یکی از چهار dNTP در مخلوط واکنش حضور دارد همانند سازی بسیار کم بوده و قطعات بیرون زده باقی میمانند. آنها به صورت یک ذوج خوشبخت به هم متصل میشوند در نتیجه شما وکتورهایی دارید که قطعات مورد نظر در آن قرار گرفته اند. این در حالی است که این کار باعث به وجود آمدن تعدادی جای خالی در حلقه پلازمیدی نیز میشود.
اما از این اتفاق نترسید!!
هنگامی که شما پلازمیدها را به سلولهای E.coli منتقل بکنید جاهای خالی ترمیم خواهند شد. شما حتی میتوانید از ترکیبی از محصولات PCR یا محصولات ناقص PCR برای به وجود آمدن قطعات بیرون زده استفاده کنید. برای انجام این کار شما باید وکتورها و محصول PCR هضم شده به وسیله پلیمراز T4 را با هم مخلوط کرده و تک رشته ای کنید تا پلازمیدی با چهار شکاف یا فاصله تک رشته ای ایجاد کنید.
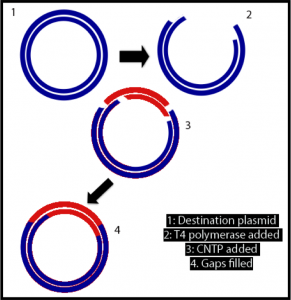
نمایی از SLIC
فرآیند SLIC میتواند لغزنده و بی ثبات باشد
اگر اکنون بسیار مشتاقید که از تکنیک SLIC استفاده کنید چند نکته مهم است که باید بدانید. مانند هر روش دیگری این روش نیز دارای تعدادی نقص است که در زیر به آنها اشاره میکنیم.
انتهای توالیهای DNA نمیتوانند ساختارهای ثانویه مناسب را مانند حلقهها و سنجاق سر که در توالیهای خاتمه یافت میشود به خود بگیرند. این ساختارها با قطعات تک رشته ای ذوب شده/متصل شده همسایه به رقابت خواهند پرداخت. در سمت مثبت، این مشکل میتواند با اضافه کردن توالیهایی از قطعات مجاور برای مقابله با انتهاهای قطعات شما بر طرف شود.
قطعات تکراری نیز میتوانند در این فرآیند مشکل ساز شوند زیرا این فرآیند متکی به همولوژی توالیها است. اتصال ناقص یا اشتباه ممکن است به دلیل شباهت دو قطعه خاص در یک انتها به وجود آید. برای فائق آمدن بر ناکارآمدی اتصال قطعات معمولا انجام اتصال متوالی پیشنهاد میشود تا قطعات چسبنده با انتهای مشابه در یک واکنش در یک زمان قرار نگیرند. به عنوان راه دیگر میتوانید توالیهای تکراری را با جفت توالیهای غیر مشابه در یک واکنش جایگزین کنید.
علاوه بر این میتوان ترکیب SLIC را با دیگر انواع واکنشهای لیگازی مشابه برای کلون کردن مانند SLICE استفاده کرد. البته اگر تنوع توالی در ۱۵ جفت باز قطعات انتهایی توالیهای اتصالی وجود داشته باشد، زیرا این کار موجب میشود نتوان از توالیهای دارای همولوژی یکسان در تمام ترکیبات استفاده کرد. اگر تشابه توالی در تمام ترکیبات و قطعات اتصالی به اندازه کافی اختصاصی باشد تا محدودیتی ایجاد نکند میتوانید از ترکیب SLIC با دیگر واکنشها استفاده کنید.
با تمام این احوال آیا با واکنشهای آنزیمی محدود شونده خداحافظی خواهید کرد؟
برای مشاهده جزئیات کامل دستورالعمل به منبع مراجعه فرمایید
منبع: Nature Methods

